|
1. Dénomination du médicament vétérinaire
EFFIPRO DUO 50 MG/60 MG SOLUTION POUR SPOT-ON POUR CHATS
2. Composition qualitative et quantitative
Une pipette de 0,50 mL contient : | | | | Substance(s) active(s) : | | Fipronil
| 50,00 mg | Pyriproxifène
. | 60,00 mg | | | Excipient(s) : | | Butylhydroxyanisole (E320)
| 0,10 mg | Butylhydroxytoluène (E321)
| 0,05 mg |
Pour la liste complète des excipients, voir rubrique «Liste des excipients».
3. Forme pharmaceutique
Solution pour spot-on. Solution limpide, incolore à jaune pâle.
4. Informations cliniques
4.1. Espèces cibles
4.2. Indications d'utilisation, en spécifiant les espèces cibles
Chez les chats : A utiliser contre les infestations par les puces seules ou les infestations mixtes par les puces et les tiques. Puces : Traitement et prévention des infestations par les puces (Ctenocephalides felis). Une application empêche toute nouvelle infestation pendant 5 semaines. Prévention de la multiplication des puces pendant 12 semaines après application, en empêchant le développement des ufs en puces adultes. Le produit peut être intégré à une stratégie de traitement de la Dermatite par Allergie aux Piqûres de Puces (DAPP) quand cette affection a fait préalablement lobjet dun diagnostic par un vétérinaire. Tiques : Traitement des infestations par les tiques (Ixodes ricinus et Rhipicephalus turanicus). Après une application, lefficacité acaricide persiste pendant une semaine. Si des tiques sont présentes au moment de lapplication, elles peuvent ne pas être toutes tuées dans les 48 heures.
4.3. Contre-indications
Ne pas utiliser chez le lapin, des effets indésirables et parfois même le décès peuvent survenir. Ne pas utiliser en cas d'hypersensibilité connue aux substances actives ou à l'un des excipients.
4.4. Mises en garde particulières à chaque espèce cible
Deux études de laboratoire ont évalué lefficacité du produit lorsque le pelage est mouillé 2 heures avant application du produit et 2 fois au cours de la période defficacité du produit contre les puces (à deux semaines dintervalle contre les puces adultes ou à quatre semaines dintervalle contre les stades immatures de puces). Mouiller le pelage dans les conditions décrites naffecte pas lefficacité du produit. Leffet dun shampoing sur lefficacité du produit na pas été évalué. Si un shampoing savère nécessaire, il est recommandé de le faire avant application du produit. Dès le début des mesures de contrôle antiparasitaire, en cas d'infestation, le panier de l'animal et ses zones de couchage ou de repos (tapis, canapés
) doivent être traités avec un insecticide approprié et passés régulièrement à laspirateur. Pour réduire la pression parasitaire environnementale liée aux puces, il est recommandé de traiter tous les animaux du foyer avec un produit contre les puces approprié. Le produit nempêche pas les tiques de se fixer. Si lanimal a été traité avant lexposition aux tiques, ces dernières seront tuées dans les 48 heures après fixation. Cela précède généralement le gorgement, réduisant mais nexcluant pas le risque de transmission de maladies. Une fois mortes, les tiques se détachent souvent de l'animal. Toute tique restante devra être retirée précautionneusement, en sassurant que les pièces buccales ne restent pas dans la peau.
4.5. Précautions particulières d'emploi
i) Précautions particulières d'emploi chez l'animal
A usage externe exclusivement. Ne pas administrer oralement. Les animaux doivent être pesés avec précision avant le traitement. En l'absence de données, le produit ne doit pas être utilisé chez les chats de moins de 10 semaines ou pesant moins de 1 kg. Eviter tout contact avec les yeux de lanimal. Dans le cas dun contact oculaire accidentel, nettoyer les yeux à leau. Veiller à appliquer le produit correctement selon la description dans la rubrique « Posologie et voie d'administration ». Ne pas appliquer le produit sur une plaie ou autre lésion cutanée. Il est important de sassurer que le produit est appliqué directement sur une zone de peau sèche que lanimal ne peut pas lécher et que les animaux ne se lèchent pas mutuellement après le traitement. Lutilisation du produit na pas été étudiée chez les animaux malades ou affaiblis. Lutilisation du produit chez les animaux malades ou affaiblis ne doit se faire quaprès évaluation du rapport bénéfice/risque établie par le vétérinaire. En l'absence d'études d'innocuité complémentaires, lintervalle minimum entre deux traitements doit être de 4 semaines.
ii) Précautions particulières à prendre par la personne qui administre le médicament vétérinaire aux animaux
Le produit peut occasionner des troubles nerveux. Le produit peut être toxique en cas dingestion. Eviter dingérer le produit ou de porter la main à la bouche après utilisation. Eviter tout contact avec la peau ou la bouche. Ne pas fumer, boire ou manger pendant lapplication du produit. Se laver les mains après utilisation. En cas dingestion accidentelle, consulter immédiatement un médecin et lui présenter la notice ou lemballage. En cas de contact accidentel avec la peau, laver immédiatement la zone touchée à leau. Ne pas toucher et ne pas laisser les enfants jouer avec les animaux traités tant que le site dapplication nest pas sec. Il est donc recommandé de ne pas traiter les animaux pendant la journée mais plutôt en début de soirée et les animaux une fois traités ne doivent pas être autorisés à dormir avec leurs maîtres, en particulier les enfants. Conserver les pipettes dans leur emballage dorigine et les éliminer immédiatement après utilisation de façon appropriée.
iii) Autres précautions
Le produit peut avoir des effets indésirables sur les surfaces, matériaux et meubles de la maison. Attendre que le site dapplication soit sec avant de permettre le contact avec ces matériaux.
4.6. Effets indésirables (fréquence et gravité)
Des modifications daspect transitoires, notamment un aspect mouillé ou une légère desquamation, peuvent être observées au site d'application. Selon l'expérience accumulée sur les substances actives administrées sous forme de spot-on, des réactions cutanées locales transitoires (desquamation, alopécie, prurit, érythème, altération de la couleur de la peau), ainsi quun prurit ou une alopécie généralisés peuvent être observés. Dans de très rares cas, une hypersalivation, des symptômes neurologiques réversibles (hyperesthésie, abattement, autres signes nerveux), des troubles respiratoires ou des vomissements peuvent survenir.
4.7. Utilisation en cas de gravidité, de lactation ou de ponte
Les études de laboratoire réalisées sur le fipronil et le pyriproxifène nont mis en évidence aucun effet tératogène ou embryotoxique. Aucune étude na été réalisée avec ce produit chez des chattes gravides ou allaitantes. L'utilisation du produit chez les chattes gestantes ou allaitantes ne doit se faire qu'après évaluation du rapport bénéfice/risque par un vétérinaire.
4.8. Interactions médicamenteuses et autres formes d'interactions
4.9. Posologie et voie d'administration
Spot-on. Posologie : Pour un chat pesant de 1 à 6 kg, appliquer une pipette de 0,5 mL, correspondant à la dose minimale recommandée de 8,3 mg de fipronil et 10 mg pyriproxifène par kg de poids corporel. Poids | Volume de la pipette | Fipronil (mg) | Pyriproxifène (mg) | 1-6 kg | 0,5 mL | 50 | 60 | >6-12 kg | 1 mL | 100 | 120 |
Pour les chats de plus de 6 kg, la dose recommandée de 1 mL doit être appliquée, ce qui peut être fait en appliquant 2 pipettes de 0,5 mL. Mode dadministration : Extraire la pipette de la plaquette thermoformée. La tenir en position verticale. Tapoter la partie étroite de la pipette pour s'assurer que le contenu est bien descendu dans la partie centrale de la pipette. Rompre l'extrémité autocassable de la pipette en suivant la ligne gravée. Ecarter les poils de l'animal à la base du cou, jusquà ce que la peau soit visible. Placer l'embout de la pipette directement sur la peau ainsi exposée. Presser doucement la partie centrale de la pipette plusieurs fois pour en expulser entièrement le contenu en un ou deux points. Sassurer que la solution est appliquée sur une peau saine. Eviter lapplication superficielle sur le pelage du chat ou que la solution ne sécoule. 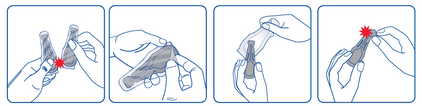 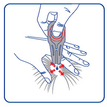
Système anti-goutte (le produit est libéré uniquement par pression sur la partie centrale de la pipette). 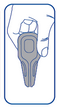 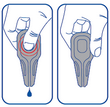
Pour un contrôle optimal des infestations par les puces et les tiques et de la multiplication des puces, la fréquence d'application peut se baser sur les conditions épidémiologiques locales. Cependant, en labsence détudes complémentaires, ne pas renouveler le traitement à intervalles de moins de 4 semaines (voir rubrique « Surdosage (symptômes, conduite d'urgence, antidotes), si nécessaire »).
4.10. Surdosage (symptômes, conduite d'urgence, antidotes), si nécessaire
Aucun effet indésirable grave n'a été observé au cours d'une étude dinnocuité réalisée sur des chatons de 10 semaines, traités avec jusquà 5 fois la dose maximale recommandée 3 fois à 4 semaines d'intervalle, et traités avec la dose maximale recommandée 6 fois à 4 semaines d'intervalle. Le risque deffets indésirables (voir rubrique « Effets indésirables (fréquence et gravité) ») peut cependant augmenter avec le surdosage, il faut donc toujours traiter les animaux avec la taille de pipette adaptée à leur poids.
4.11. Temps d'attente
5. Propriétés pharmacologiques
Groupe pharmacothérapeutique : Antiparasitaire à usage externe (association de fipronil ). Code ATC-vet : QP53AX65.
5.1. Propriétés pharmacodynamiques
Le fipronil est un insecticide et un acaricide de la famille des phénylpyrazolés. Le fipronil et son métabolite, le fipronil sulfone, agissent sur les canaux chlorure activés par des ligands, en particulier les canaux activés par le neurotransmetteur acide gamma-aminobutyrique (GABA) mais aussi les canaux désensibilisants (D) et non-désensibilisants (N) activés par le glutamate (Glu, canaux chlorure ligand-dépendants propres aux Invertébrés). Ils bloquent ainsi le passage pré- et post-synaptique des ions chlorure à travers la membrane cellulaire. Il en résulte une activité incontrôlée du système nerveux central et la mort des insectes ou des acariens. Le pyriproxifène est un inhibiteur de croissance des insectes (IGR) de la famille des analogues de l'hormone juvénile. Le pyriproxifène stérilise les puces adultes et inhibe le développement des stades immatures. La molécule empêche, par contact, l'émergence d'insectes adultes, en bloquant le développement des ufs (effet ovicide), des larves et des pupes (effet larvicide), qui sont ainsi éliminés. Elle agit également par contact et/ou ingestion par les puces adultes en stérilisant les ufs pendant leur maturation et avant la ponte. Enfin, la molécule empêche la contamination de l'environnement des animaux traités par les stades immatures des puces. L'association du fipronil et du pyriproxifène présente une activité insecticide et acaricide contre les puces (Ctenocephalides felis) et les tiques (Rhipicephalus turanicus, Ixodes ricinus) et empêche le développement des ufs en puces adultes. Une telle association procure un contrôle intégré des puces qui peut être utilisé lors dinfestations par les puces seules ou lors dinfestations mixtes par les puces et les tiques.
5.2. Caractéristiques pharmacocinétiques
Dans les conditions normales dutilisation, le fipronil et le pyriproxifène sont correctement distribués dans le pelage de l'animal dès le premier jour suivant lapplication topique. Le métabolite principal du fipronil est son dérivé sulfoné, qui possède également des propriétés insecticides et acaricides. Les concentrations de fipronil et de pyriproxifène dans le pelage diminuent progressivement mais sont toujours détectables au moins 84 jours après application (cest-à-dire au-dessus de la limite inférieure de quantification qui est de 100 ng/g pour le fipronil et de 50 ng/g pour le pyriproxifène). Les concentrations de fipronil sulfone restent en dessous de la limite inférieure de quantification (LQ 100 ng/mL) après lapplication du produit. Le pic de concentration plasmatique du fipronil et du pyriproxifène est rapidement atteint 1 jour après administration du produit. Les concentrations de fipronil sont quantifiables chez tous les chats jusquà 3 jours après application (LQ 1 ng/mL). Les concentrations de pyriproxifène sont quantifiables chez tous les chats jusquà 42 jours après application (LQ 0,2 ng/mL). Les concentrations de fipronil sulfone restent en dessous de la limite inférieure de quantification (LQ 1 ng/mL) après application du produit.
6. Informations pharmaceutiques
6.1. Liste des excipients
Butylhydroxyanisole (E320) Butylhydroxytoluène (E321) Ether monoéthylique de diéthylèneglycol
6.2. Incompatibilités
6.3. Durée de conservation
Durée de conservation du médicament vétérinaire tel que conditionné pour la vente : 3 ans.
6.4. Précautions particulières de conservation
Ne pas conserver à une température supérieure à 30°C. Conserver dans un endroit sec. Conserver les plaquettes thermoformées dans leur emballage extérieur pour les protéger de la lumière.
6.5. Nature et composition du conditionnement primaire
Pipette thermoformée unidose plastique transparente (polyacrylonitrile méthacrylate-polypropylène-copolymère doléfines cycliques-polypropylène) et thermoscellé par film polyacrylonitrile méthacrylate-aluminium-polyéthylène téréphtalate
Pipette placée dans plaquette thermoformée (polypropylène-copolymère d'oléfines cycliques-polypropylène) et thermoscellée par film polyéthylène téréphtalate-aluminium-polypropylène
6.6. Précautions particulières à prendre lors de l'élimination de médicaments vétérinaires non utilisés ou de déchets dérivés de l'utilisation de ces médicaments
Les conditionnements vides et tout reliquat de produit doivent être éliminés suivant les pratiques en vigueur régies par la réglementation sur les déchets. Ne pas contaminer les étangs, les cours deau ou les fossés avec le médicament ou les emballages vides car ils peuvent nuire aux poissons et autres organismes aquatiques.
7. Titulaire de l'autorisation de mise sur le marché
VIRBAC
1ERE AVENUE 2065 M L I D
06516 CARROS CEDEX
FRANCE
8. Numéro(s) d'autorisation de mise sur le marché
FR/V/6206131 9/2015
Boîte de 1 pipette de 0,5 mL
Boîte de 4 pipettes de 0,5 mL
Boîte de 24 pipettes de 0,5 mL
Boîte de 60 pipettes de 0,5 mL
Toutes les présentations peuvent ne pas être commercialisées.
9. Date de première autorisation/renouvellement de l'autorisation
10. Date de mise à jour du texte
| 
